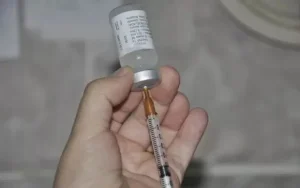
Da Redação – A partir da segunda quinzena de novembro, o Sistema Único de Saúde (SUS) passará a disponibilizar a vacina contra o vírus sincicial respiratório (VSR), principal causador da bronquiolite e responsável por cerca de 60% dos casos de pneumonia em crianças menores de dois anos.
O VSR circula com maior intensidade nos meses de inverno e está associado a complicações respiratórias como bronquite, bronquiolite e pneumonia. Entre 2018 e 2024, essas condições levaram a 83 mil internações de bebês prematuros no país. Segundo especialistas, a imunização materna permitirá que anticorpos sejam transferidos para o bebê ainda na gestação, oferecendo proteção imediata no período mais vulnerável da vida.
Estima-se que a vacina possa evitar cerca de 28 mil internações anuais e beneficiar aproximadamente 2 milhões de recém-nascidos. Dados do Ministério da Saúde mostram que, a cada cinco crianças infectadas pelo VSR, uma precisa de atendimento ambulatorial e, em média, uma em cada 50 é hospitalizada durante o primeiro ano de vida. O risco é ainda maior entre os prematuros, cuja taxa de mortalidade é sete vezes superior à de crianças nascidas a termo.
As primeiras 1,8 milhão de doses serão adquiridas por meio de acordo entre o Instituto Butantan e a farmacêutica Pfizer, com entrega prevista até dezembro. Inicialmente, o governo federal enviará 832,5 mil doses para os estados em novembro e, até o fim do ano, mais 1 milhão.
O ministro da Saúde, Alexandre Padilha, destacou que a medida representa um marco para a saúde pública:
“É uma proteção dupla: protege a gestante e o recém-nascido. E, ao mesmo tempo, garante transferência de tecnologia, incorporação de inovação e geração de emprego, renda e conhecimento ativo no nosso país”.
O Comitê Técnico Assessor do Ministério da Saúde recomenda a aplicação de uma dose a partir da 28ª semana de gestação, em linha com as orientações da Organização Mundial da Saúde (OMS). A pasta também acompanhará a necessidade de reforços em futuras gestações.
A vacina contra o VSR é uma novidade no mundo. A primeira a ser aprovada foi a Arexvy, da farmacêutica britânica GSK, liberada nos Estados Unidos em maio de 2023, inicialmente indicada apenas para pessoas com 60 anos ou mais.